LIAISONS SÉRIE – LIAISONS PARALLÈLE « 2ème PARTIE »
ASSOCIATION DE PILES
Après avoir vu ce qui se produit dans le circuit extérieur des piles, selon le type de liaison adopté pour les résistances, nous allons examiner le circuit intérieur aux piles.
Le courant qui retourne aux pôles négatif de la pile, après avoir parcouru le circuit extérieur, doit traverser la solution électrolytique à l’intérieur de la pile pour se porter sur le pôle positif, d’où il recommence à circuler dans le circuit extérieur.
La solution électrolytique de la pile offre une résistance au courant qui la traverse. Comme cette résistance n’appartient pas au circuit extérieur, elle est appelée résistance interne de la pile.
Figure 9, la partie située à gauche des points A et B constitue le circuit interne de la pile.
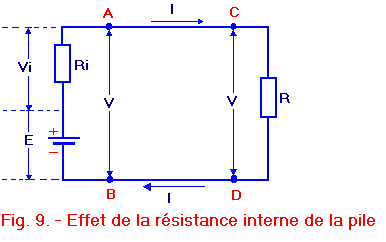
La pile possédant une résistance interne, il est possible de la matérialiser sur le circuit électrique, c’est ce que nous avons fait avec la résistance Ri.
Si nous considérons cette résistance Ri comme une résistance à part entière, étant traversée par le courant I, une tension Vi va naître à ses bornes. Ri produit une chute de tension mais comme Ri est située à l’intérieur de la pile, cette chute de tension s’effectue dans la pile. C’est pour cette raison que la résistance et la chute de tension qu’elle provoque sont symbolisées par un i, (i servant à rappeler que ces deux paramètres sont internes à la pile).
En conséquence, la tension nécessaire aux bornes de la pile n’est pas la tension totale fournie par la pile, mais est égale à cette tension diminuée de la chute de tension interne.
Selon la loi d’Ohm, la tension qui apparaît aux bornes de Ri s’obtient en multipliant Ri par le courant qui la traverse, or ce courant n’est autre que le courant traversant le circuit et fourni par la pile.
Nous constatons donc que la chute de tension interne à la pile est d’autant plus élevée que le courant débité par celle-ci augmente.
Inversement, cette chute de tension interne est nulle quand la pile n’est reliée à aucun circuit extérieur. Dans de telles conditions, aux bornes de la pile apparaît la totalité de la tension qu’elle peut fournir.
Cette tension s’appelle force électromotrice d’une pile et est symbolisée par la lettre E comme dans la figure 9.
Il faut retenir de ceci que la force électromotrice d’une pile est la tension présente à ses bornes lorsque la pile ne fournit aucun courant. L’unité de la force électromotrice est bien sûr le volt.
Dans la plupart des cas, la résistance interne d’une pile est de loin très inférieure à la résistance du circuit extérieur et lors d’éventuels calculs, cette valeur est négligée sans que cela apporte d’erreur appréciable dans les résultats.
Dans ces cas, nous considérons que la tension fournie par la pile est égale à sa force électromotrice. Dorénavant, pour le terme force électromotrice, nous utiliserons l’abréviation universellement reconnue f.e.m.(Nous reportons le même circuit pour vous faciliter la tâche).

Pour illustrer ce qui vient d’être dit, donnons des valeurs aux éléments de la figure 9 :
E = 9 V
Ri = 0,3 Ohm
R = 8,7 Ohms
Le courant I circulant dans le circuit est donné par le rapport entre la f.e.m. et la résistance équivalente de ce circuit constitué de R et de Ri.
I = E / Req = E / R + Ri = 9 V / 0,3 + 8,7 = 9 / 9 = 1 A
La chute de tension Vi interne à la pile est de :
La tension disponible aux bornes de la résistance R lorsque la pile débite un courant de 1 A est de :
V = E – Vi = 9 – 0,3 = 8,7 V
Comme vous pouvez le constater, la tension chutée dans Ri est minime au regard de la tension réellement disponible aux bornes de R. Pour d’autres calculs, Vi pourrait donc être négligée.
Voyons à présent les différentes associations réalisables à partir de plusieurs piles.
Figure 10 est représenté le type d’association que vous serez appelé à rencontrer le plus souvent, il s’agit d’une association en série.
Cette association s’effectue en reliant la borne positive de l’une à la borne négative de l’autre. Puisque chaque pile a une f.e.m. de 1,5 V entre les points B et A, il y a une différence de potentiel de 1,5 V de même qu’entre les point C et B.
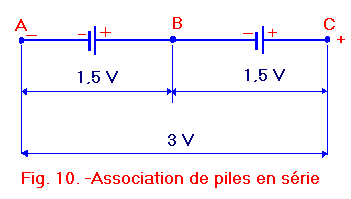
Le point C a un potentiel électrique supérieur de 1,5 V à celui du point B, qui lui-même a un potentiel supérieur de 1,5 V par rapport au point A. Nous aurons donc un potentiel électrique de 3 V entre les points C et A, bornes de l’ensemble.
Nous pouvons alors conclure :
En mettant plusieurs piles en série, on obtient une f.e.m. totale égale à la somme des f.e.m. de chaque pile.
On a recours à ce type d’association lorsque l’on a besoin d’une tension plus élevée que celle fournie par une seule pile. Dans ce cas, l’ensemble des piles reliées en série est aussi appelé batterie de piles. Ceci est le cas de la pile de 4,5 V que vous utilisez pour vos pratiques puisqu’elle est formée de trois éléments de 1,5 V chacun reliés en série.
En ce qui concerne la résistance interne, il est évident qu’une batterie de piles a une résistance interne égale à la somme des résistances internes de chaque élément qui la compose. Enfin, tous les éléments étant en série, ils sont traversés par le même courant, comme dans toutes les associations de ce type. D’autre part, il faut savoir qu’une pile ne doit jamais fournir un courant d’intensité supérieure à une valeur déterminée, qui dépend de ses caractéristiques de fabrication, sous peine d’entraîner rapidement sa détérioration.
C’est pour cela que le circuit extérieur d’une pile n’est jamais constitué par un simple fil de cuivre:en effet, à cause de la très faible résistance du fil, la pile serait obligée de fournir un courant d’intensité très élevée qui la détériorerait très vite. Dans ce cas, on dit que la pile est en court-circuit; pour la bonne conservation des piles, il faut donc éviter de les mettre en court-circuit, en reliant directement leurs pôles par un simple conducteur de résistance négligeable.
Quand un courant plus important que celui que peut délivrer une seule pile est nécessaire, nous utilisons plusieurs piles reliées en parallèle comme le montre la figure 11.
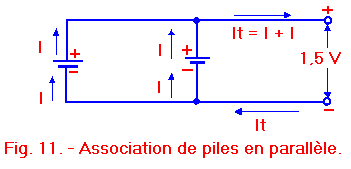
Dans cette figure,nous voyons que le courant total fourni par plusieurs piles en parallèle est égal à la somme des courants que peut fournir chaque pile.
Naturellement, pour que cela se produise, il faut que les pôles positifs de chaque pile soient reliés entre eux, de même que les pôles négatifs, comme sur la figure 11. Aux bornes de l’ensemble, la f.e.m. est égale à celle fournie par une seule pile, caractéristique commune à toutes les associations en parallèle.
En pratique, ce type d’association est rarement utilisé parce que si les résistances internes et les f.e.m. de chaque pile ne sont pas rigoureusement identiques, on observera la décharge d’une pile dans l’autre entraînant leur détérioration mutuelle.
Laisser un commentaire